淋巴循环构建病原体体内扩散途径及宿主抵抗机制
日期:2018-11-07
巴尔通体由节肢动物的叮咬传播感染哺乳动物,形成持续性菌血症及杆菌性血管瘤。巴尔通体在节肢动物肠道内增殖,随其粪便排出到被叮咬哺乳动物的皮肤表面,通过表皮的伤口快速感染进入宿主动物血液红细胞内,建立持续性感染。由于上皮屏障、皮下天然免疫细胞及淋巴结系统作用,通常病原体无法通过表皮性的伤口达到深部器官感染。但巴尔通体如何在表皮伤口感染后2小时内即感染血液红细胞的特殊机制一直未有研究阐明。
袁聪俐课题组在2013年在权威期刊《Journal of Infectious Diseases》发表论文“Depolymerization of cytokeratin intermediate filaments facilitates intracellular infection of HeLa cells by Bartonella henselae”, 证明巴尔通体通过结合细胞角蛋白6解聚了细胞中间纤维,破坏了上皮细胞间的致密结合结构,促进巴尔通体快速通过细胞间隙进入淋巴循环,首次阐明了巴尔通体突破上皮屏障的机制。随后课题组与第一人民医院李岩课题组通力合作,构建了胸导管淋巴液引流模型,成功的证明了巴尔通体在淋巴结内阻断了巨噬细胞炎性焦亡反应,在淋巴结内建立免疫沉默在皮下感染后1小时即侵入淋巴循环,并通过淋巴管与前腔静脉的交汇处进入血液循环感染红细胞,形成持续性的菌血症;伴随着节肢动物的吸血叮咬进入第二个感染循环。该研究结果于2017年在权威期刊《Journal of Infectious Diseases》发表论文“Lymphatic Circulation Disseminates Bartonella Infection Into Bloodstream.”。在皮下感染阶段,巴尔通体将其效应蛋白bepE注射入树突状细胞内(DCs)促进细胞快速迁移进入淋巴结,挟持宿主细胞作为木马促进巴尔通体体内扩散。基于该现象,袁聪俐课题组随后与加州大学旧金山分校,北京大学等单位合作,证明宿主细胞内泛素化系统对效应蛋白bepE中4个位点的赖氨酸残基进行多泛素化修饰,尤其是K63的多泛素修饰激活了细胞的自噬反应,降解细胞内bepE,抑制其对细胞迁移及内吞活性的调控,阐明了宿主细胞利用泛素自噬系统反制细菌效应蛋白的工作机制。该研究论文“Bartonella quintana Type IV secretion effector BepE induced selective autophagy by conjugation with K63 poly-ubiquitin chain”在2018年收录于权威期刊《Cellular Microbiology》。
上述研究成果得到了国家自然科学基金、上海市科委政府间国际合作基金等项目的支持。
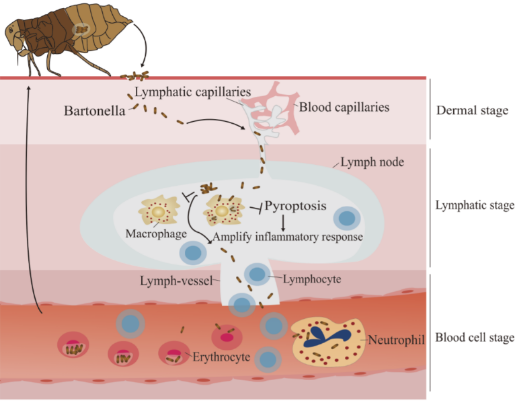
巴尔通体在节肢动物-哺乳动物感染循环及免疫调控机制